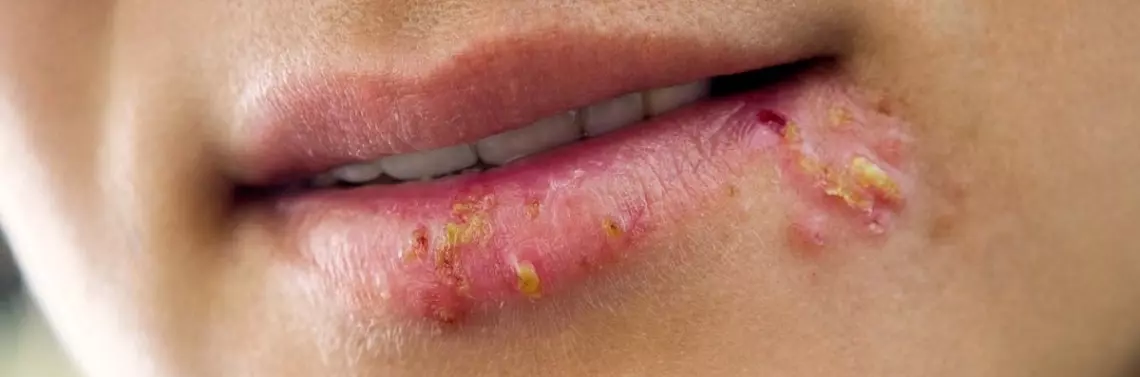
Choroba Duhringa (zapalenie opryszczkowate skóry, dermatitis herpetiformis – DH) jest schorzeniem zaliczanym do pęcherzowych podnaskórkowych chorób autoimmunologicznych. Choroba Duhringa jest schorzeniem przewlekłym, przebiegającym z okresami remisji i nawrotów. Choroba występuje przede wszystkim u osób rasy białej, w Europie najczęściej w Finlandii. Zapalenie opryszczkowate skóry może się pojawić w każdym wieku, ale większość przypadków dotyczy młodych dorosłych w wieku od 15 do 40 lat. Po raz pierwszy została opisana przez Louisa Adolphusa Duhringa w 1884 r. [1]. Choroba Duhringa wymaga różnicowania z innymi schorzeniami z kręgu chorób pęcherzowych. Jednak najczęściej schorzenie jest mylone ze zmianami wypryskowatymi i atopowym zapaleniem skóry. Etiopatogeneza DH nie jest w pełni poznana, najprawdopodobniej choroba ma podłoże autoimmunologiczne. Głównym czynnikiem środowiskowym zaangażowanym w wywołanie choroby jest ekspozycja na gluten. Zmiany skórne mają charakter swędzących polimorficznych wykwitów skórnych, którym towarzyszy enteropat...
Pozostałe 90% treści dostępne jest tylko dla Prenumeratorów
- Roczną prenumeratę dwumiesięcznika Food Forum w wersji papierowej lub cyfrowej,
- Nielimitowany dostęp do pełnego archiwum czasopisma,
- Możliwość udziału w cyklicznych Konsultacjach Dietetycznych Online,
- Specjalne dodatki do czasopisma: Food Forum CASEBOOK...
- ...i wiele więcej!

Dołącz do grona dietetyków i specjalistów świadomego żywienia
Co dwa miesiące otrzymuj gotowe rozwiązania, aktualne badania i sprawdzone terapie, które możesz od razu wykorzystać w praktyce. Rozwijaj swoje kompetencje, pracuj skuteczniej i bądź na bieżąco z najnowszymi trendami żywieniowymi i innowacjami w dziedzinie dietetyki.